![]()
Kupfer(II)-sulfat-Pentahydrat
ist für den Menschen nur leicht giftig und ruft bei Verschlucken Brechreiz hervor.
Der Stoff ist für Mikroorganismen stark giftig und darf nicht in Gewässer gelangen.
Ammoniakwasser (Salmiakgeist)
ist für Menschen giftig. Ammoniak wird vornehmlich über die Atmung aufgenommen
und verätzt die Atemwege was bis zum Atemstillstand führen kann. Beim Umgang
ist auf gute Lüftung zu achten.
Ammoniumhydrogencarbonat
ist als Lebensmittelzusatzstoff E503ii als Hirschhornsalz im Handel. Es wird
als Backtriebmittel für Lebkuchen verwendet und wird als gesundheitsgefährdend
eingestuft, weil es beim Erhitzen Ammoniak abspaltet.
Kupfer(II)-sulfat-Pentahydrat:
Apotheke
Kraft Keramikbedarf, Leinburg,
http://www.keramik-kraft.de/DE/Rohstoffe_-_Spezialprod_/Rohstoffe-_Carbonate-_Oxide/Rohstoffe_und_Oxide/Kupfersulfat_X-aetzend__Bt_100_g_R394-01.html?sel=96
Ammoniakwasser (Salmiakgeist):
Farbenfachhandel
Ammoniumhydrogencarbonat:
Supermarkt im Backregal
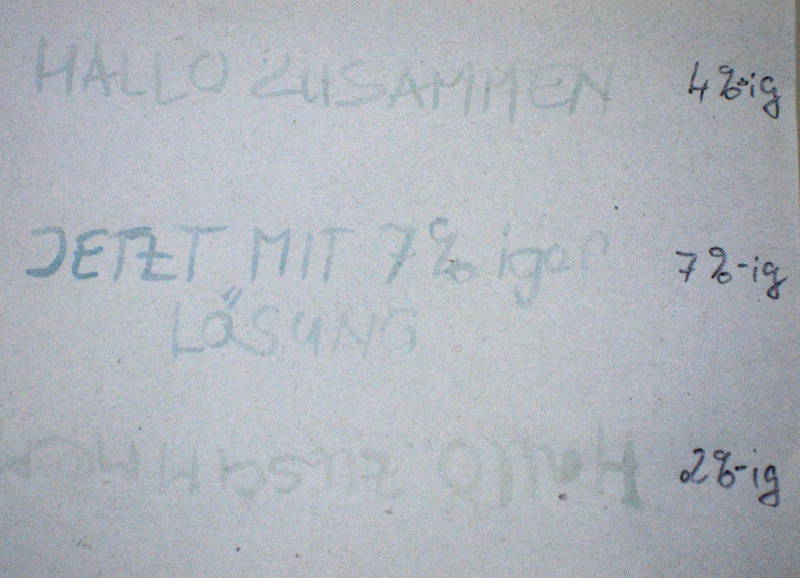
Abb. 1: Versuche mit verschiedenen Konzentrationen von wässriger Kupfersulfatlösung
(nach Ammoniakeinwirkung)

Abb. 2: Ca. 0,2g Kupfer(II)-Sulfat-Pentahydrat
0,2g Kupfersulfat wird in 10cm³ Wasser in einem kleinen Schraubglas durch Schütteln gelöst. Die 2%-ige Lösung wird mit einem spitzen Pinsel, der nicht zu viel Flüssigkeit enthalten soll, auf leicht blau-grau-farbiges Papier aufgetragen.
Es ist vorteilhaft, wenn das Papier nicht glatt ist sondern eine leichte Struktur aufweist. Weißes stark geleimtes Papier ist ungeeignet, weil man dort den Schriftauftrag an den matten Stellen erkennen würde wo das Papier aufquillt. Anschließend lässt man die Schrift trocknen.
Zum Schreiben darf keine Stahlfeder verwendet werden! Durch Elektrolyse würde an der Feder elementares Kupfer abgeschieden, das mit in die Schrift fließt. Zum einen ist die Schrift dann durch die Verschmutzung lesbar und zum anderen würde der Farbumschlag schwächer ausfallen, weil Ammoniak mit Kupfer nicht reagiert.
Zum Sichtbarmachen hält man das Papier mit der beschrifteten Seite nach unten über die geöffnete Flasche mit Salmiakgeist. Gut lüften, Ammoniakdämpfe nicht einatmen!
Ersatzweise kann man auch Hirschhornsalz in einem Kaffeelöffel über einer Teelichtflamme erhitzen. In der Hitze zerfällt das Ammoniumhydrogencarbonat in Ammoniak, Kohlenstoffdioxid und Wasser. Ammoniak und Kupfersulfat verbinden sich daraufhin zu Tetraminkupfersulfat, wodurch die Schriftzüge dunkelblau hervortreten.
Durch weiteres Hinzufügen von Kupfersulfat zur vorhandenen Lösung wurde die Konzentration schrittweise gesteigert. Dabei wurde darauf geachtet, dass die Schrift zunächst unsichtbar blieb, aber nach der Behandlung mit Ammoniak dennoch deutlicher hervortrat. Es stellte sich heraus, dass dies für Konzentrationen um die 10% noch problemlos möglich ist.


Abb. 3: 10%-ige Kupfersulfatlösung Abb.
4: Geschrieben mit 10%-iger Kupfersulfatlösung
Interessant ist, dass die Blaufärbung wieder zurückgeht, wenn man das Papier längere Zeit an der Luft liegen lässt. Das geht bei niedrigen Konzentrationen fast bis zur völligen Entfärbung. Die Schrift wird wieder gut lesbar, wenn man sie erneut mit Ammoniak behandelt.
![]()